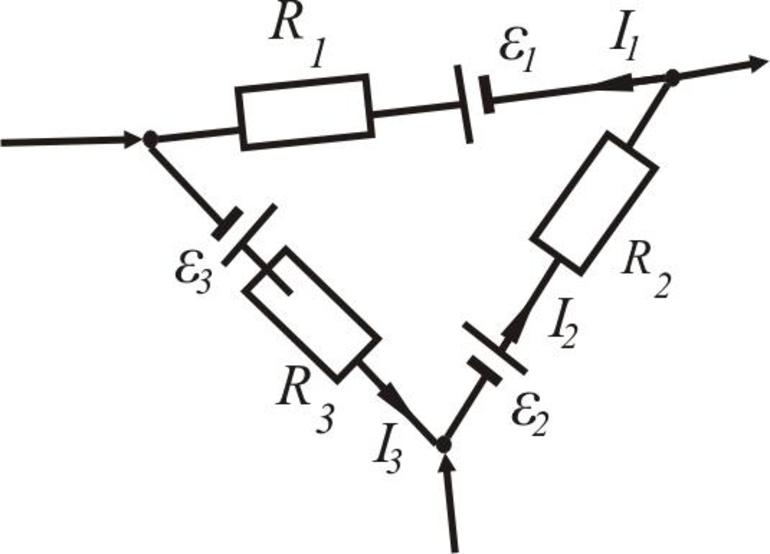
Правило Кирхгофа - функции и примеры применения первого и второго правил
В физике присутствует несколько видов задач на законы Кирхгофа, где требуется найти либо силу тока, либо ЭДС источника энергии в гальванической цепи.
Примеры разобранных задач на правила Кирхгофа:


- Дана электрическая схема, на которой изображены источники ЭДС и 3 резистора, соединенных параллельно. Необходимо найти величину силы тока в цепи, если указаны значения сопротивления и электродвижущей силы. Изначально нужно определить количество узлов и составить уравнение на основе первого закона. В этом случае входящие и выходящие потоки энергии считаются равными по модулю, но разными по направлению. Затем составляются уравнения с использованием второго закона, учитывая значение ЭДС и сопротивления. После составления уравнения для всех контуров образуется система. Финальным шагом является подстановка известных величин в уравнение.
- Дана гальваническая схема, где отображены 5 резисторов и гальванометров. Известны сопротивления 4 из них. Требуется найти силу тока для 1 — 4 резисторов и ЭДС для 4 гальванометра, если известна величина тока для 5 источника. В начале составляется уравнение для первого закона. Получится 2 равенства. После составляются уравнения по второму правилу. Получается 3 равенства для аналогичного количества контуров. В результате получится система из 5 уравнений. Финальным этапом является решение системы с подстановкой известных значений.
Все задачи на законы Кирхгофа решаются методом составления уравнений, основываясь на 2 законах. Проверка результата осуществляется при помощи баланса мощностей.
Во время проведения вычислений рекомендуется использовать онлайн-калькуляторы для работы с большими числами.
Законы Кирхгофа в химии
Кирхгоф в течение долгого времени занимался изучением химии, исследуя тепловые явления. Ученый разработал закон для определения коэффициента температуры при выделении теплоты во время осуществления химической реакции. Оно справедливо как для органических, так и для неорганических веществ. Для описания закона вводятся понятия изобарной и изохорной емкости, обозначаемые символами CP и CV. Закон гласит, что температурный коэффициент химической реакции эквивалентен амплитуде изменения теплоемкости.

В дифференциальной форме закон определяет зависимость изменения теплового эффекта от повышения или понижения температуры. Величина теплового эффекта высчитывается при помощи закона Гесса, где учитывается тип реакции. Тепловыделение будет увеличиваться при эндотермических реакциях, уменьшаться — при экзотермических реакциях.
Во время расчета температуры важно учитывать агрегатное состояние, истинную или среднюю теплоемкость, качественный состав и вид веществ, смешанных в растворе. Эти характеристики являются табличными величинами и указаны в химических справочниках. На основе полученных данных составляется уравнение, устанавливающее аналитическую зависимость теплового эффекта от значения температуры.