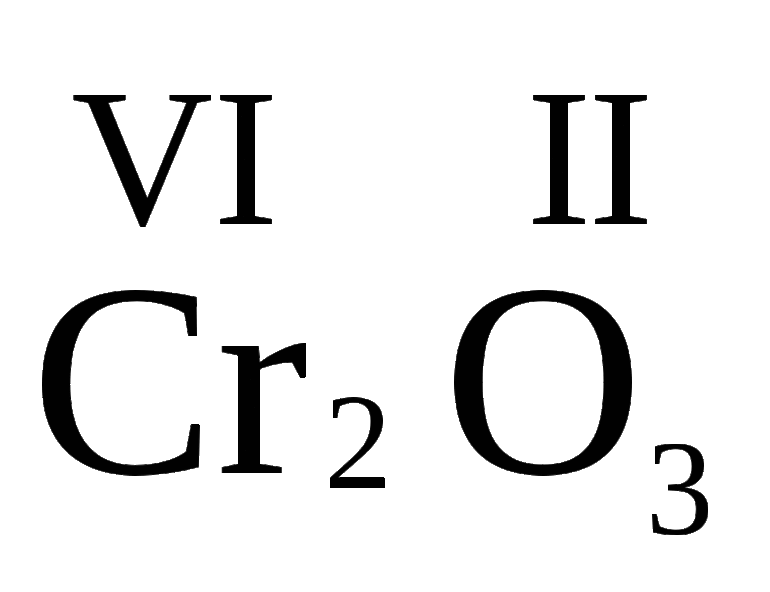Валентность химических элементов
В школе на уроках химии рассказывается о подробном строении элементов, атомов. Существует понятие валентности химических элементов, имеющее смысл для веществ молекулярной природы. Показатель бывает постоянный и переменный, изменяющийся в зависимости от соединений. Мерной единицей является число связей, образующих мелкие частицы с остальными атомами или их группами.
Содержание: