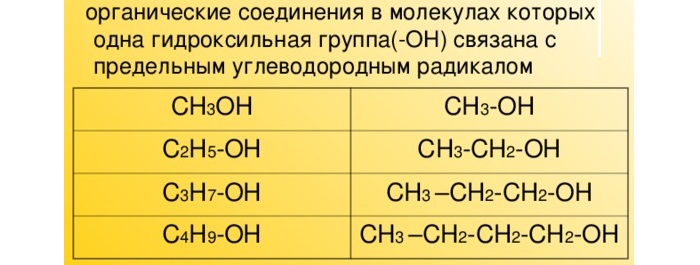
Одноатомные спирты - строение, классификация и свойства
Вещества с количеством атомов углерода до 15 являются летучими жидкостями с резким запахом. Соединения с числом атомов углерода свыше 15 являются твердыми веществами.

Начальный член гомологического ряда (метанол) чрезвычайно токсичен для человека.
Чем выше спирт, тем и выше его температура кипения. Различия между каждым членом гомологического ряда составляет примерно 20 градусов. По мере увеличения размера молекулы и ее массы снижается и их воспламеняемость. Следовательно, легче всех воспламеняется метанол.
Соединения, имеющие в составе молекулы 9 атомов углерода, растворяются в воде (метанол и этанол – в каком угодно соотношении). Хорошо растворяются в растворителях.
Химические свойства
Рассматриваемые вещества ведут себя и как основания, и как кислоты.
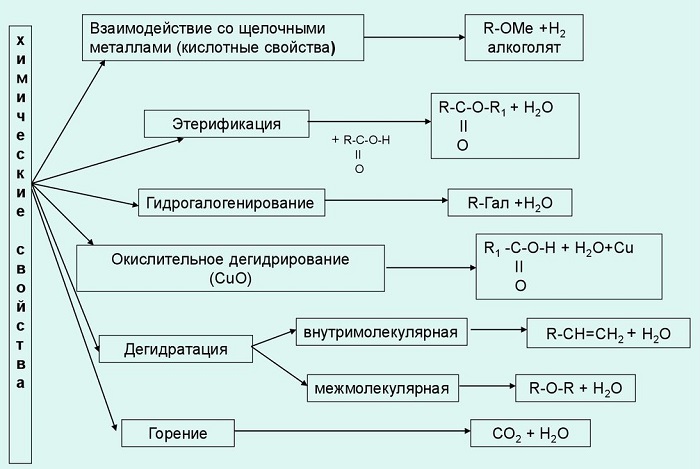
Основные химические свойства одноатомных спиртов:
-
Взаимодействие с щелочными металлами. При этом образуются алкоголяты или алкоксиды. В воде эти вещества подвергаются гидролизу, образуя спирт и основание.
-
Взаимодействие с кислотами (органическими и неорганическими). По-другому они называются реакциями этерификации, поскольку конечный их продукт - сложный эфир.
-
Реакция с хлористым тионилом дает в итоге галогеналкан.
-
В результате внутримолекулярного обезвоживания получают алкены.
-
При межмолекулярной дегидратации образуются простые эфиры.
-
Химическая реакция одноатомного алкоголя с перманганатом калия дает альдегид. Дальнейшим окислением альдегида можно получить одноатомную карбоновую кислоту.
Получение

Известно несколько методов получения простых спиртов:
1. Гидратация алкенов (с присоединением молекулы воды):
CH2 = CH2 + H2O → CH3CH2OH.
2. Гидролиз алкилгалогенидов (с добавлением водных растворов щелочей):
CH3CH2Сl + NaOH → CH3CH2OH + NaCl.
3. Восстановление кетонов:
CH3-C(O)-CH3 + Н2 → CH3-CH(CH)-CH3.
4. Этанол получают путем разложения глюкозы:
C6H12O6 → 2C2H5OH + 2CO2.
5. Восстановление карбоновых кислот и сложных эфиров.
6. Присоединение металлорганических химических соединений к кетонам и альдегидам.
Применение одноатомных спиртов
Одноатомные спирты широко применяются как исходный реагент для получения альдегидов, кетонов, карбоновых кислот и эфиров. Все эти вещества широко применяются в производстве и быту.
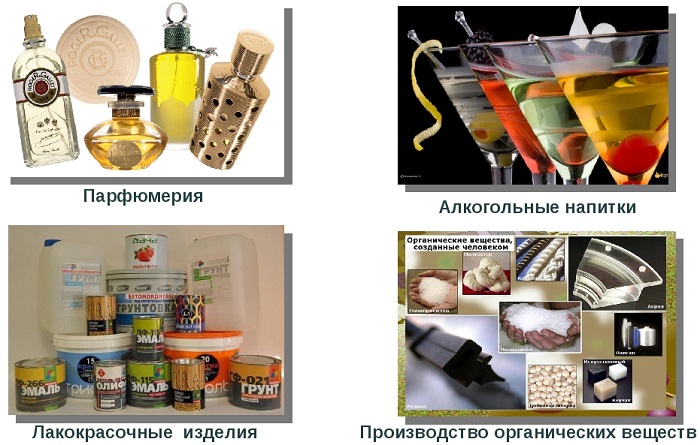
Вот примеры использования наиболее распространенных спиртов:
-
Метанол является прекрасным органическим растворителем. Его применяют в производстве лаков и красок, органических смол.
-
Этанол широко используется в медицине как антисептик и растворитель. В пищевой промышленности его используют для получения алкогольных напитков. Он является основой для получения сложных эфиров, уксуса.
-
Бутанол применяется как растворитель и основа для получения веществ с приятным ароматом.
-
Бензиловый спирт является основой для получения душистых веществ.
Рассмотренные в статье вещества имеют широкое применение в промышленности. Без них невозможно получение многих веществ, использующихся в быту.