Серная кислота - формула, свойства и уравнения реакций
В индустриальных масштабах синтезируют так называемым контактным методом. Пирит (серный колчедан) при интенсивном нагревании выделяет среди прочих продуктов разложения сернистый газ. Из реактора также выходят водяные испарения и насыщенный кислородом воздух (подается).
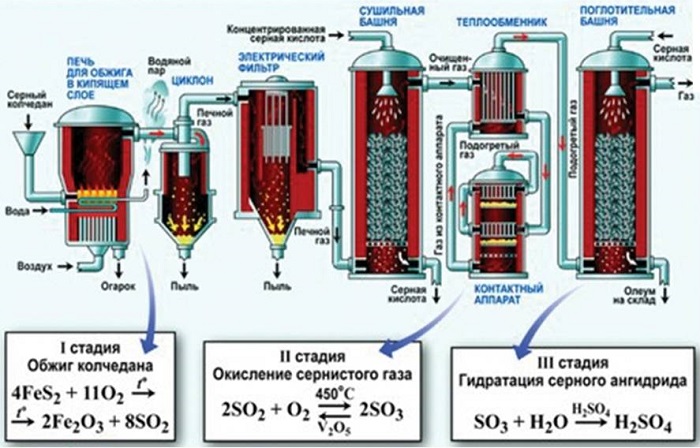
Полученная смесь очищается от посторонней взвеси и влаги. В контактном агрегате производится окисление до серного ангидрида. В присутствии катализатора и под давлением. Триоксид в дальнейшем поглощается концентрированной кислотой. На выходе полагается олеум.
Воду для растворения не практикуют из-за обильного тепловыделения. Это усложняет производство.
Основным потребителем являются производители минеральных удобрений (порядка 70%). В химической промышленности применяются для синтеза искусственных волокон, красок.
Используются для выделки кож. В пищевых добавках. В значимых для РФ отраслях. Очистка и переработка нефти, производство порохов и взрывчатки. Для металлообрабатывающих комплексов.
Дополнительную привлекательность создает доступность сырья. Важны также простота и дешевизна получения.







