Типы кристаллических решеток
Физические и химические свойства кристаллических неметаллов зависят от того, чем образована их кристаллическая решетка — атомами или молекулами, и их взаимодействием. Атомные или немолекулярные связи очень прочные, молекулярные — слабые.
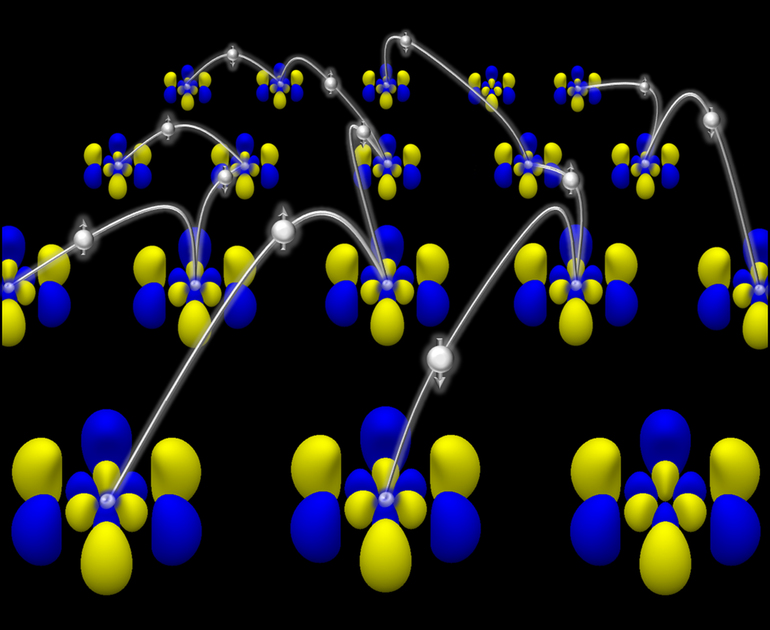
Между соседними атомами образуются совместные электронные пары, при этом каждый из них остается устойчивым элементом. Связь, созданная в таких парах, называется ковалентной (или прочной). Когда взаимодействуют атомы с одинаковой электроотрицательностью, то расположение электронной пары получается симметричным относительно двух атомов и называется ковалентной неполярной связью.
У веществ, состоящих из разных неметаллов, связь образовывается из атомов с разной электроотрицательностью, в результате чего общая электронная пара смещается к более отрицательному элементу. Получается ковалентная полярная связь.
Соединения с ковалентными связями бывают двух типов — молекулярными и атомными.
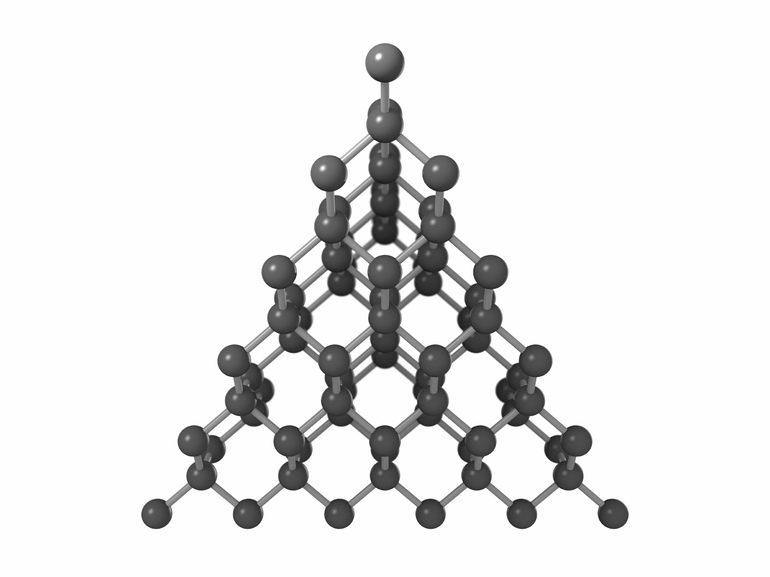
Структуры, в узлах которых размещаются атомы, соединенные ковалентными связями, называются атомными кристаллическими решетками. Если связь ковалентная неполярная, то в ее формировании участвуют атомы одного химического вещества. Такую структуру имеют кремний Si, бор B, германий Ge, кристаллические видоизменения углерода C. Геометрическое строение решетки кристалла имеет соответствие с его свойствами.
Например, две модификации углерода: алмаз и графит. В кубической структуре алмаза атомы расположены по одному в вершинах, по центру каждой грани, и четыре внутри самого куба. Это строение дает самую плотную упаковку атомов, а ковалентные связи между ними делает очень прочными. Поэтому алмаз является самым твердым материалом в мире. Другие свойства: теплопроводность низкая, электрический ток не проводит.

У графита гексагональная слоистая решетка, которая делает его мягким. Температура плавления очень высокая (4 тыс. градусов Цельсия), обладает электропроводностью, его называют полуметаллом и используют при производстве электродов.
При биполярной ковалентной связи атомная кристаллическая решетка обычно сформирована атомами разных химических элементов. Такое строение имеют муассанит, состоящий из кремния Si и углерода C, и диоксид кремния SiO2 в разных модификациях:
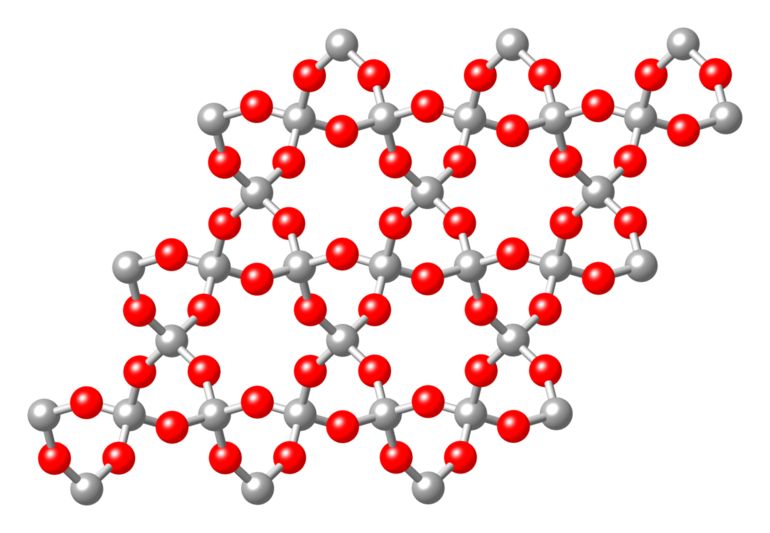
- кварцевый песок;
- лютецит;
- опал;
- халцедон;
- хрусталь;
- кремнезем.
Основные свойства: нерастворимость, прочность, твердость, высокие температуры плавления и кипения.
Молекулярное строение
Структуры, образованные полярными молекулами, между которыми существуют силы взаимодействия, называются молекулярными кристаллическими решетками. Межмолекулярные связи в них имеют электрическую природу, для их разрыва не требуется много энергии. В то же время атомы этих молекул ковалентны.
К веществам, имеющим молекулярное строение, относятся:
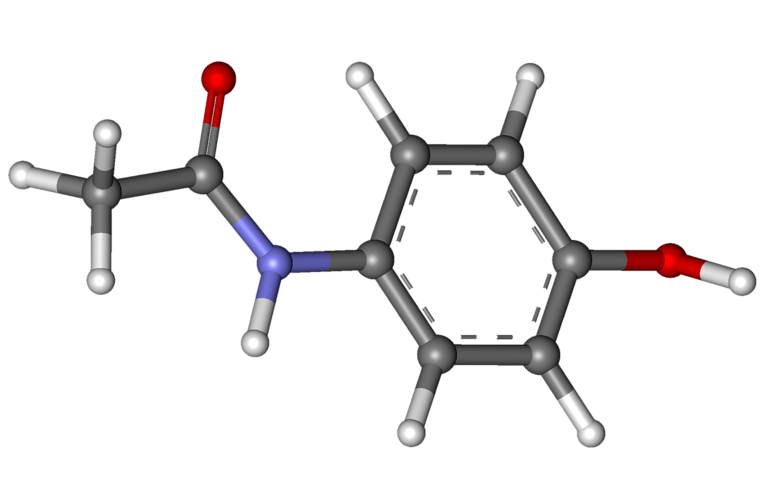
- белый фосфор, моноклинная и ромбическая сера;
- галогены, галогеноводороды и другие жидкости и газы в твердом агрегатном состоянии (йод, фтор, хлор, азот, кислород, озон, вода, оксид углерода — так называемый сухой лед);
- инертные газы с одноатомными молекулами (неон, аргон, ксенон).
Такое строение соответствует и большинству органических соединений.
Слабое взаимодействие между молекулами определяет свойства веществ, имеющих такое строение. Они мягкие и непрочные, имеют низкие температуры плавления и кипения. Эти кристаллы обладают летучестью, хорошо растворяются в воде и других жидкостях.
Благодаря разнообразию пространственных схем кристаллов, из одних и тех же химических элементов можно получить значительно отличающиеся друг от друга материалы.







